Khái niệm Phân tử, nguyên tử, hình dạng, sự khác nhau và một số ví dụ
Trong chương trình hóa học, các bạn đã từng được tìm hiểu phân tử là gì đúng không? Vậy nhưng có một số bạn vẫn chưa nắm được “phân tử là gì”, hãy theo dõi bài viết này Studytienganh.vn để biết phân tử là gì nhé!
Phân tử là một nhóm trung hòa điện tích có từ 2 nguyên tử trở lên, liên kết với nhau bằng những liên kết hóa học.
Bạn đang xem: Khái niệm Phân tử, nguyên tử, hình dạng, sự khác nhau và một số ví dụ
Phân tử sẽ được phân biệt với ion do thiếu điện tích. Trong vật lý lượng tử, hóa sinh và hóa học hữu cơ, thuật ngữ phân tử được sử dụng không quá nghiêm ngặt, cũng áp dụng cho các ion đa nguyên tử.
Theo lý thuyết động học của chất khí, khái niệm phân tử được dùng cho bất kỳ hạt khí nào bất kể thành phần của nó. Theo khái niệm này, các nguyên tử khí trơ cũng được coi là các phân tử bởi chúng là các phân tử đơn phân tử.
( Hình ảnh về phân tử trong hóa học )
Một phân tử cũng có thể là hạt nhân, tức là nó gồm các nguyên tử của một nguyên tố, ví dụ như với oxy (O2). Bên cạnh đó, nó có thể là một hợp chất hóa học nhiều hơn một nguyên tố, ví dụ là nước (H2O).
Ví dụ cụ thể về một phân tử điển hình là phân tử nước. Phân tử nước là gì? Kí hiệu ra sao? Phân tử nước là sự kết hợp hợp của 2 nguyên tử Hydro (H+) cad 1 nguyên tử Oxy (O2-). Công thức hóa học của nước là H2O.
Kích thước của phân tử này siêu nhỏ, trong đó H+ cũng là nguyên tử nhỏ nhất trong các nguyên tố. Vì vậy, nước thẩm thấu vào da rất dễ dàng. Do điện tích trái dấu giữa nguyên tử Hidro và Oxy, các phân tử nước thường hút nhau bằng liên kết Hidro. Nhưng liên kết này không bền vững, dễ đứt gãy. Ngoài ra, một số phân tử khác cũng rất phổ biến như Nitơ (N2), Canxi Oxit (CaO), Ôzon (O3), Glucozo (C6H12O6), Muối ăn (NaCl).
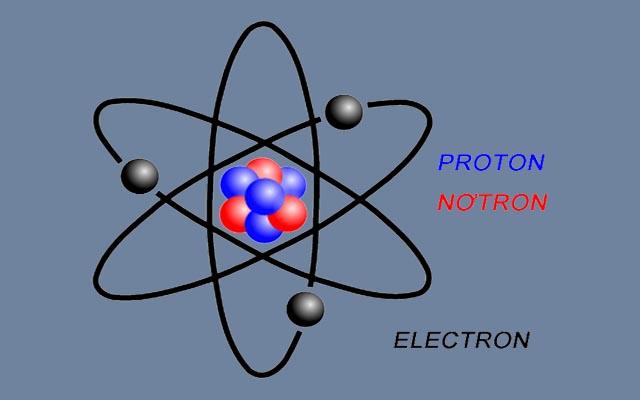
Nguyên tử là hạt siêu nhỏ và trung hòa về điện. Thành phần nguyên tử bao gồm hạt nhân nguyên tử (Proton và Notron) và vỏ nguyên tử (Electron). Khối lượng của nguyên tử bằng khối lượng của hạt nhân nguyên tử.
( Hình ảnh minh họa về “nguyên tử” trong hóa học )
Từ các kết quả thực nghiệm, các nhà khoa học đã xác định được thành phần cấu tạo nguyên tử gồm có hạt nhân và lớp vỏ electron.
Trong đó:
=> Nguyên tử được cấu tạo bởi 3 loại hạt cơ bản là: electron, proton và nơtron.
Cơ sở để so sánh
Xem thêm : Thịt thăn heo làm món gì ngon? Bật mí 10 món ngon dễ làm – Digifood
Nguyên tử
Phân tử
Ý nghĩa
Hạt nhỏ của một nguyên tố hóa học, có thể tồn tại hoặc không tồn tại độc lập được gọi là nguyên tử.
Các phân tử đề cập đến tập hợp các nguyên tử được liên kết với nhau bằng liên kết, chỉ ra đơn vị nhỏ nhất của hợp chất.
Sự tồn tại
Có thể hoặc không tồn tại ở trạng thái tự do.
Tồn tại trong trạng thái tự do.
Bao gồm
Hạt nhân và điện tử.
Hai hoặc nhiều hơn, các nguyên tử giống hệt nhau hoặc khác nhau, liên kết hóa học.
Hình dạng
Hình cầu
Tuyến tính, góc và tam giác
Tầm nhìn
Xem thêm : Quan hệ với bạn gái 17 tuổi có phải chịu trách nhiệm hình sự?
Không nhìn thấy được bằng mắt thường, cũng không phải kính hiển vi.
Không thể nhìn thấy bằng mắt thường, nhưng có thể được nhìn thấy với sự trợ giúp của kính hiển vi.
Khả năng phản ứng
Phản ứng cao, có ngoại lệ nhất định
Tương đối ít phản ứng.
Liên kết
Liên kết hạt nhân
Liên kết cộng hóa trị
Bài tập 1: Nguyên tử của nguyên tố X có tổng số hạt là 40. Tổng số hạt mang điện nhiều hơn số hạt không mang điện là 12 hạt. Nguyên tử X có số proton là?
Lời giải:
Nguyên tử của nguyên tố X có tổng số hạt là 40 thì số hạt = p + e + n = 2p + n = 40 (1)
Số hạt mang điện sẽ nhiều hơn số hạt không mang điện là 12
=> p + e – n = 2p – n = 12 (2)
Từ (1) và (2) => p = 13; n = 14
Vậy số proton có trong nguyên tử X bằng 13
Trên đây là những thông tin, kiến thức về “phân tử là gì”, chúc các bạn có những kiến thức về phân tử thật hiệu quả cùng studytienganh.vn nhé
Nguồn: https://luatduonggia.edu.vn
Danh mục: Tổng hợp
This post was last modified on 28/02/2024 19:49
Con số may mắn hôm nay 23/11/2024 theo năm sinh: Nhặt TIỀN từ con số…
Tử vi thứ bảy ngày 23/11/2024 của 12 con giáp: Tuổi Thìn chán nản, tuổi…
Vận may của 4 con giáp đang ngày càng xuống dốc. Cuối tuần này (23-24/11),…
Con số cuối cùng trong ngày sinh dự đoán con người sẽ GIÀU CÓ, sống…
Cuối tuần này (23-24/11), 4 con giáp sẽ gặp nhiều may mắn và thành công…
Tử vi hôm nay – Top 3 con giáp thịnh vượng nhất ngày 22/11/2024