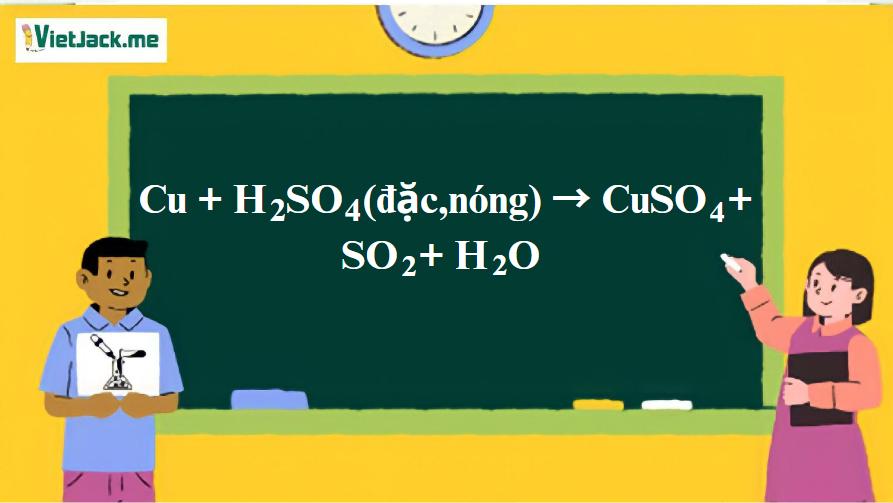
Cu + H2SO4 (đặc,nóng) → CuSO4 + SO2 + H2O | Cu ra CuSO4
Phản ứng: Cu + H2SO4 (đặc,nóng) → CuSO4 + SO2 + H2O
1. Phương trình phản ứng hóa học
Cu + 2H2SO4 → CuSO4 + SO2 + 2H2O
2. Hiện tượng nhận biết phản ứng.
– Chất rắn màu đỏ Đồng (Cu) tan dần trong dung dịch và sủi bọt khí do khí mùi hắc Lưu huỳnh dioxit (SO2) sinh ra.
3. Điều kiện phản ứng
– Nhiệt độ
4. Bản chất của các chất tham gia phản ứng
4.1 Bản chất của Cu
Bản chất của Cu trong phản ứng là chất khử
4.2 Bản chất của H2SO4
Axit sunfuric đặc có tính axit mạnh, oxi hóa mạnh
5. Tính chất hóa học của Cu
5.1 Tác dụng với phi kim:
Cu phản ứng với oxi khi đun nóng tạo CuO bảo vệ nên Cu không bị oxi hoá tiếp tục.
Xem thêm : Dưới bao nhiêu điểm thì thi lại? Những quy định thi lại mà học sinh cần phải biết
2Cu + O2 CuO
Khi tiếp tục đun nóng tới (800-1000oC)
CuO + Cu Cu2O (đỏ)
Tác dụng với Cl2, Br2, S…
Cu + Cl2 CuCl2
5.2 Tác dụng với axit:
Khi có mặt oxi, Cu tác dụng với dung dịch HCl, nơi tiếp xúc giữa dung dịch axit với không khí.
2Cu + 4HCl + O2 → 2CuCl2 + 2 H2O
Cu + 2H2SO4 đ → CuSO4 + SO2 + H2O
Cu + 4HNO3 đ → Cu(NO3)2 + 2NO2 + 2H2O
3Cu + 8HNO3 loãng → 3Cu(NO3)2 + 2NO + 4H2O
5.3 Tác dụng với dung dịch muối
Khử được ion kim loại đứng sau nó trong dung dịch muối.
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
6. Tính chất hóa học của H2SO4 đặc
Axit sunfuric đặc có tính axit mạnh, oxi hóa mạnh với tính chất hóa học nổi bật như:
Xem thêm : Quy định hát karaoke đến mấy giờ
6.1 Tác dụng với kim loại: Khi cho mảnh Cu vào trong H2SO4 tạo ra dung dịch có màu xanh và có khí bay ra với mùi sốc.
Cu + 2H2SO4 → CuSO4 + SO2 + 2H2O
6.2 Tác dụng với phi kim tạo thành oxit phi kim + H2O + SO2.
C + 2H2SO4 → CO2 + 2H2O + 2SO2 (nhiệt độ)
2P + 5H2SO4 → 2H3PO4 + 5SO2 + 2H2O
6.3 Tác dụng với các chất khử khác.
2FeO + 4H2SO4 → Fe2(SO4)3 + SO2 + 4H2O
C12H22O11 + H2SO4 → 12C + H2SO4.11H2O
7. Tính chất vật lí của H2SO4 đặc
– Tồn tại dưới dạng chất lỏng, không màu, không mùi và không vị.
– H2SO4 đặc nổi bật với khả năng hút nước rất mạnh và tỏa nhiều nhiệt. Vì vậy bạn chú ý không nên cho nước vào axit mà chỉ được phép cho axit vào nước. Để đánh trường hợp bị bỏng xảy ra khi nước tác dụng với axit. Và H2SO4 còn có thể pha loãng ra để trở thành H2SO4 lỏng.
8. Cách thực hiện phản ứng
– Cho vào ống nghiệm 1,2 lá đồng, nhỏ từ từ vừa đủ dung dịch H2SO4 đặc, sau đó đun nóng nhẹ ống nghiệm
9. Bạn có biết
– H2SO4 đặc, nóng tác dụng với đồng, sinh ra khí lưu huỳnh đioxit SO2 và dung dịch CuSO4 màu xanh lam.
10. Bài tập liên quan
Nguồn: https://luatduonggia.edu.vn
Danh mục: Tổng hợp
This post was last modified on 12/04/2024 07:25
Vận mệnh người tuổi Mùi theo cung hoàng đạo: Bạn có dễ thăng tiến không?
Hé lộ vận mệnh 12 con giáp tháng 12/2024: Những rủi ro nào đang rình…
Cẩm nang may mắn năm 2025 cho người tuổi Tý: Cơ hội đổi đời trong…
Tử vi hôm nay 4 con giáp ngày 26/11/2024 gặp nhiều may mắn, vận may…
Con số may mắn hôm nay 26/11/2024 theo tuổi sinh: Hãy chọn SỐ ĐÚNG để…
Tử vi thứ ba ngày 26/11/2024 của 12 con giáp: Tý xui xẻo, Mùi an…